Grafen ve Grafen Oksit Arasındaki İletkenlik Farkları
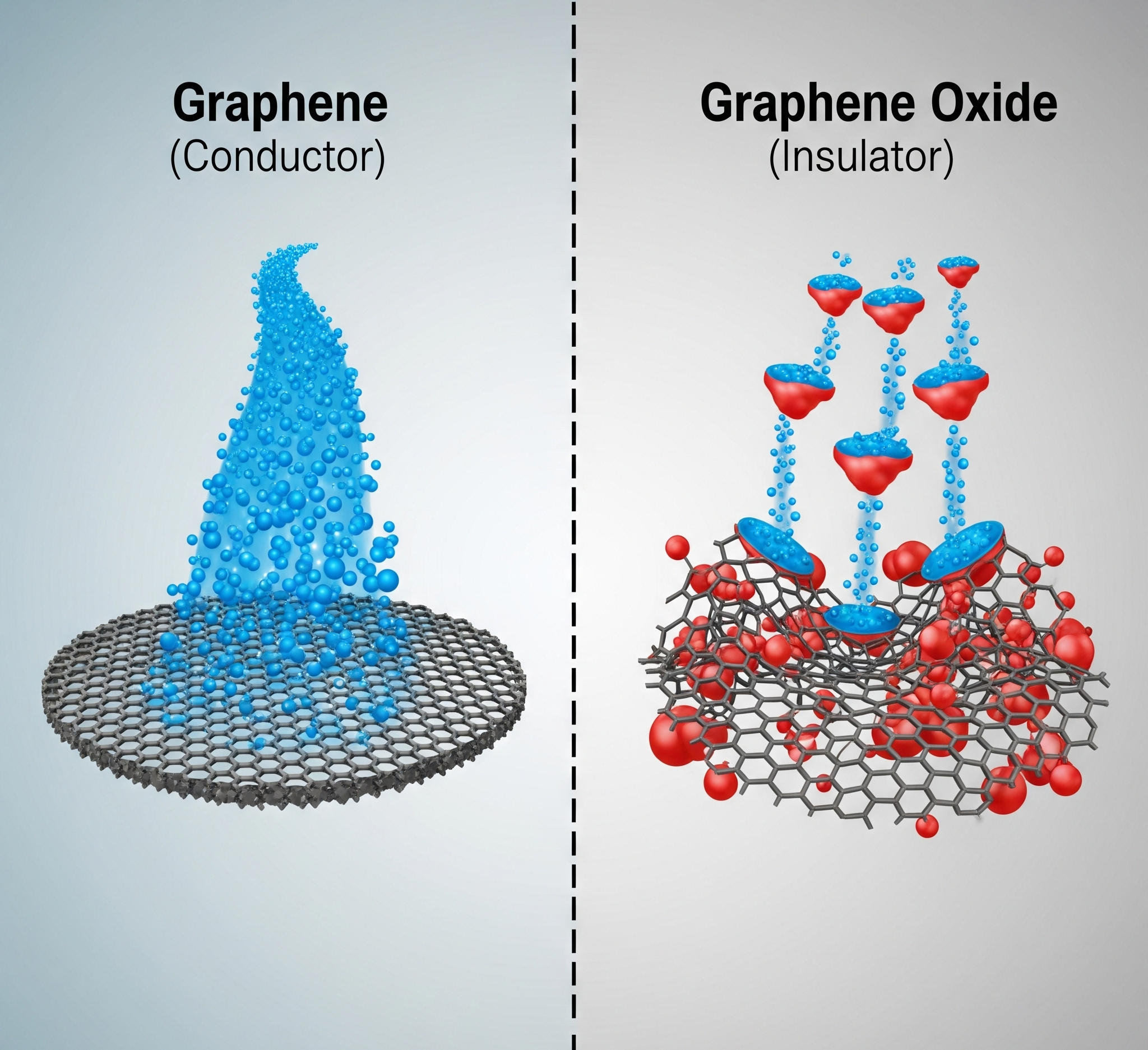
Grafen ve Grafen Oksit (GO), malzeme bilimi dünyasında sıkça birlikte anılan iki isim. Her ikisi de grafitten türetilir ve tek atom kalınlığında tabakalardan oluşur. Ancak bu benzerlikler, en temel özelliklerinden birine gelindiğinde keskin bir şekilde ayrılır: elektriksel iletkenlik. Saf grafen, bilinen en iyi iletkenlerden biriyken, grafen oksit neredeyse tamamen bir yalıtkandır.
Peki, yapıya eklenen birkaç oksijen atomu, bir malzemeyi nasıl bir süper iletkenden bir yalıtkana dönüştürebilir? Bu sorunun cevabı, malzemelerin atomik yapısında ve karbon atomlarının kurduğu bağlarda gizlidir.
Grafen: Mükemmel Bir İletkenin Anatomisi
Grafenin olağanüstü iletkenliğini anlamak için karbon atomlarının dizilimine bakmamız gerekir.
Anahtar Kavram: sp² Hibritleşmesi ve Pi (π) Bağı Ağı
Saf grafende, her karbon atomu komşu üç karbon atomuna güçlü kovalent bağlarla bağlanır. Bu yapıya sp² hibritleşmesi denir. Bu düzenleme, bal peteği şeklinde, düzlemsel ve kararlı bir yapı oluşturur.
Her karbon atomunun dış yörüngesinde dört elektron bulunur. Üç tanesi bu sp² bağlarını oluşturmak için kullanılır. Peki, dördüncü elektron ne olur? İşte sihir burada başlar. Bu dördüncü elektron, atom düzleminin üstünde ve altında serbestçe hareket edebilen bir pi (π) bağı oluşturur.
Tüm karbon atomlarından gelen bu serbest pi elektronları birleşerek, grafen tabakasının tamamını kaplayan, kesintisiz ve hareketli bir “elektron denizi” veya “elektron otoyolu” oluşturur. Elektrik voltajı uygulandığında, bu elektronlar bu otoyolda neredeyse hiç dirençle karşılaşmadan, inanılmaz bir hızla akabilir. Grafeni süper iletken yapan şey, bu kesintisiz elektron otoyoludur.
Grafen Oksit (GO): İletkenliğin Kayboluşu
Grafen Oksit, grafitin sülfürik asit gibi güçlü oksitleyici maddelerle işlenmesiyle üretilir. Bu süreç, grafenin kusursuz yapısını temelden değiştirir.
Yapısal Devrim: sp³ Hibritleşmesi ve Fonksiyonel Gruplar
Oksidasyon sırasında, epoksi ve hidroksil gibi oksijen içeren fonksiyonel gruplar, grafen tabakasının yüzeyine rastgele bir şekilde bağlanır. Bu oksijen grupları, bağlandıkları karbon atomlarını sp² hibritleşmesinden sp³ hibritleşmesine geçmeye zorlar.
sp³ hibritleşmesi, elmasın yapısında bulunan bağ türüdür. Bu bağda, karbonun dört dış elektronu da komşu atomlarla kilitlenmiş, lokalize bağlar oluşturur. Serbest hareket edebilen bir “pi elektronu” kalmaz.
Sonuç olarak, grafen oksit tabakası, iletken sp² bölgelerinin ve yalıtkan sp³ bölgelerinin bir karışımı haline gelir. Oksijen grupları, o mükemmel “elektron otoyolu” üzerinde devasa “barikatlar” veya “çukurlar” oluşturur. Elektronlar artık tabaka boyunca serbestçe akamazlar; bu yalıtkan sp³ adacıklarına takılıp kalırlar. Bu nedenle, grafen oksit bir bütün olarak elektriksel yalıtkan gibi davranır.
Joker Kart: İndirgenmiş Grafen Oksit (rGO)
Hikaye burada bitmiyor. Grafen Oksit, kimyasal veya termal işlemlerle “indirgenerek” oksijen gruplarının büyük bir kısmı uzaklaştırılabilir. Bu yeni malzemeye İndirgenmiş Grafen Oksit (reduced Graphene Oxide – rGO) denir.
İndirgeme işlemi, sp³ bölgelerinin bir kısmını tekrar sp²’ye dönüştürerek “elektron otoyolunu” kısmen onarır. Ancak bu onarım asla mükemmel olmaz. Yapıda hala kusurlar, boşluklar ve kalan oksijen grupları bulunur. Bu nedenle rGO:
- Saf grafen gibi mükemmel bir iletken değildir.
- Grafen oksit gibi tam bir yalıtkan da değildir.
- Bir yarı iletkendir. İletkenliği, indirgenme seviyesine bağlı olarak ayarlanabilir.
Uygulamadaki Anlamı: Neden Bu Fark Önemli?
Bu temel iletkenlik farkı, bu malzemelerin hangi uygulamalar için uygun olduğunu belirler:
- Grafen: Yüksek iletkenlik gerektiren uygulamalar için idealdir.
- Ultra hızlı transistörler
- Şeffaf iletken filmler (dokunmatik ekranlar, esnek ekranlar)
- Yüksek frekanslı elektronikler
- Grafen Oksit (GO): Yalıtkan olması veya yüzey kimyasının önemli olduğu uygulamalar için kullanılır.
- Su arıtma membranları (yüzeydeki gruplar kirleticileri tutar)
- Biyomedikal uygulamalar (ilaç taşıma sistemleri)
- Kompozit malzemelerde takviye (iletkenlik gerekmez)
- İndirgenmiş Grafen Oksit (rGO): Ayarlanabilir ve orta düzeyde iletkenlik gerektiren, maliyet etkin çözümler için tercih edilir.
- Sensörler (kimyasal ve biyosensörler)
- Enerji depolama (batarya ve süperkapasitör elektrotları)
- İletken mürekkepler
Sonuç
Özetle, grafen ve grafen oksit arasındaki devasa iletkenlik farkı, atomik yapıdaki bir değişiklikten kaynaklanır. Grafenin kesintisiz sp² yapısı bir elektron otoyolu yaratırken, grafen oksitin bozulmuş sp³ yapısı bu otoyolu yok eder. Bu temel ayrımı anlamak, grafen ailesi malzemelerinin inanılmaz potansiyelini doğru teknolojik uygulamalara yönlendirmek için hayati öneme sahiptir. Seçim, hedeflenen uygulamanın bir süper iletkene mi, bir yalıtkana mı, yoksa ayarlanabilir bir yarı iletkene mi ihtiyaç duyduğuna bağlıdır.
Yorum yapabilmek için giriş yapmalısınız.


Yazar hakkında