Akıllı İlaç Taşıyıcı Sistemler ve Nanoteknoloji
Hedefe yönelik tedavi konsepti, modern tıbbı dönüştürdü. Artık ilaçları, tüm vücudu etkileyen bir “halı bombardımanı” yerine, doğrudan hastalıklı hücrelere yönlendirilen bir “akıllı füze” gibi düşünebiliyoruz. Peki ya bu akıllı füze, sadece doğru adrese gitmekle kalmayıp, aynı zamanda harekete geçmek için doğru anı bekleseydi? Ya ona “ateş” komutunu tam olarak ihtiyaç duyduğumuz anda, istediğimiz yerde verebilseydik?
İşte bu ileri düzey kontrol ve hassasiyet, akıllı ilaç taşıyıcı sistemler ile mümkün hale geliyor. Nanoteknoloji sayesinde geliştirilen bu sistemler, pasif bir şekilde hedefe gitmenin ötesine geçerek, belirli biyolojik veya dışsal sinyallere yanıt vererek taşıdıkları ilacı “isteğe bağlı” olarak serbest bırakırlar. Bu, tedavide maksimum etki ve minimum yan etki anlamına gelen yeni bir devrimin kapılarını aralıyor.
‘Akıllı’ Ne Demek? Tetikleyiciye Duyarlı Salınım
Bir ilaç taşıyıcı sistemi “akıllı” yapan şey, ilacı sürekli veya kontrolsüz bir şekilde salmak yerine, belirli bir tetikleyici (stimuli) ile karşılaştığında aktif hale gelmesidir. Bu tetikleyiciler, sistemin tasarımına göre iki ana kategoriye ayrılır:
1. Vücudun Kendi Sinyalleri: İçsel Tetikleyiciler
Bu sistemler, hastalıklı dokuların sağlıklı dokulardan farklı olan benzersiz mikro-çevresini bir anahtar olarak kullanır.
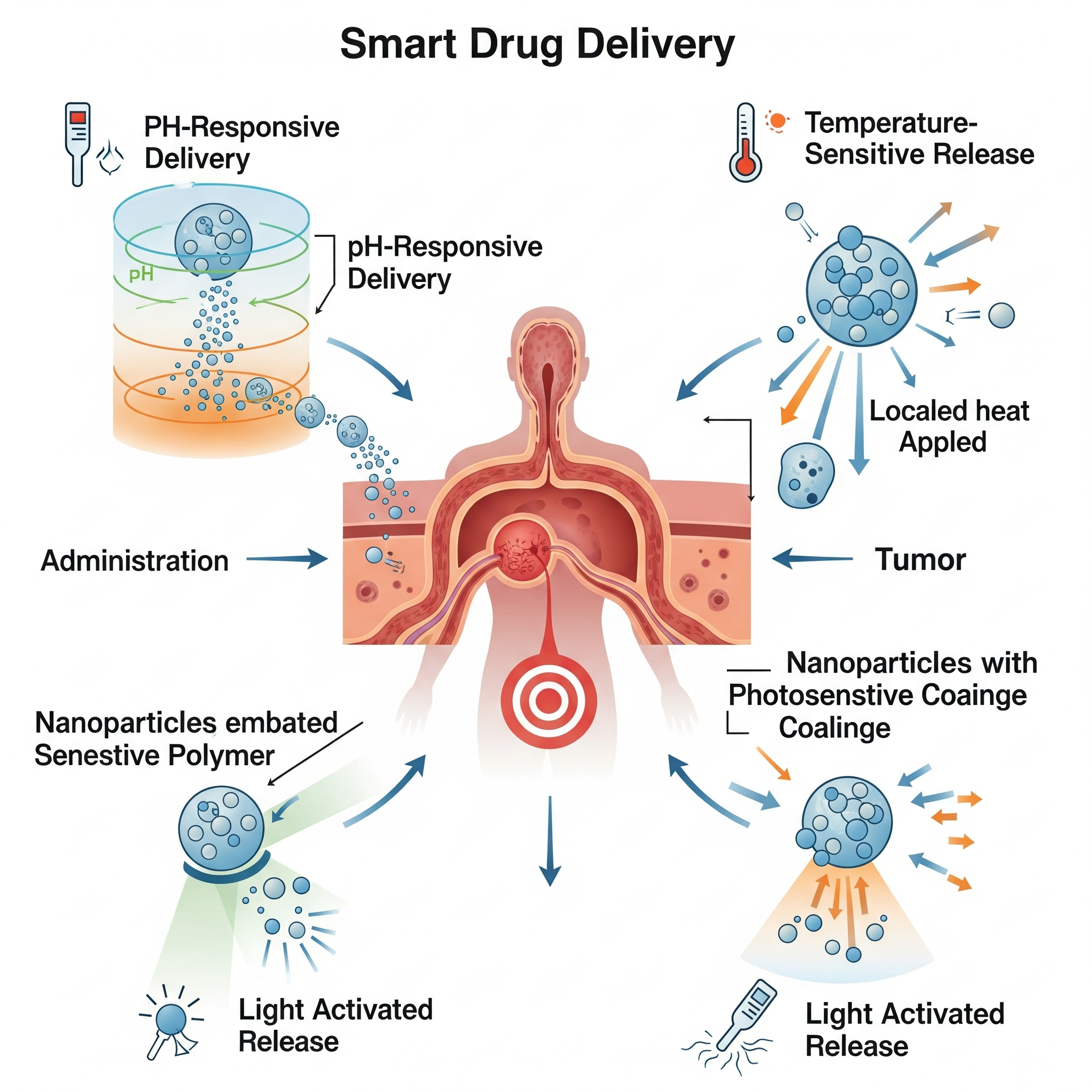
- pH Duyarlılığı: Kanserli tümörlerin çevresi, sağlıklı dokulara göre daha asidiktir (daha düşük pH’a sahiptir). pH’a duyarlı olarak tasarlanan nanotaşıyıcılar (lipozomlar, hidrojeller), normal kan dolaşımında (pH ~7.4) stabil kalır, ancak tümörün asidik ortamına (pH ~6.5) ulaştığında yapısı bozularak ilacı tam olarak hedefe bırakır. Bu, sadece asidik bir ortamda çözünen bir kapsül gibidir.
- Enzim Duyarlılığı: Bazı hastalıklar, belirli enzimlerin aşırı üretilmesine neden olur. Nanotaşıyıcılar, bu spesifik enzimler tarafından tanınıp parçalanabilen “moleküler kilitlerle” donatılabilir. Bu sayede ilaç, sadece o enzimin bol olduğu hastalıklı bölgede serbest kalır.
- Redoks Potansiyeli: Hücre içi ve hücre dışı ortam arasında kimyasal bir denge farkı vardır. Özellikle hücre içindeki yüksek glutatyon seviyeleri, redoks duyarlı taşıyıcıların bağlarını kırarak ilacın sadece hedef hücreye girdikten sonra salınmasını sağlar.
2. Dışarıdan Gelen Komutlar: Dışsal Tetikleyiciler
Bu yaklaşım, doktora tedavi üzerinde anlık ve doğrudan bir kontrol imkanı sunar.
- Sıcaklık: Sıcaklığa duyarlı polimerlerden yapılan nanotaşıyıcılar, vücut sıcaklığında (37°C) kararlıdır. Odaklanmış ultrason veya manyetik alan gibi yöntemlerle tümör bölgesi lokal olarak 40-42°C’ye ısıtıldığında, bu taşıyıcılar büzüşerek veya eriyerek içindeki ilacı hızla serbest bırakır.
- Işık (Fototermal Tetikleme): Dokuya derinlemesine nüfuz edebilen yakın kızılötesi (NIR) ışık, ışığa duyarlı nanomalzemeleri (örneğin altın nanoparçacıklar) aktive etmek için kullanılabilir. Dışarıdan uygulanan bu ışık, taşıyıcının ısınmasını veya yapısının değişmesini sağlayarak kontrollü bir ilaç salınımı tetikler.
- Manyetik Alan: Manyetik nanoparçacıklar, dışarıdan uygulanan bir manyetik alanla hem doğrudan tümör bölgesine yönlendirilebilir hem de değişken bir manyetik alan uygulanarak ısıtılarak veya titreştirilerek ilacın salınması sağlanabilir.
Akıllı İlaç Taşıyıcılarının Potansiyel Uygulamaları
Bu teknoloji, sadece kanser tedavisinde değil, birçok alanda çığır açma potansiyeline sahiptir:
- Kanser Tedavisi: Kemoterapi ilaçlarını sadece tümörde ve en etkili olacağı anda serbest bırakarak sistemik toksisiteyi ortadan kaldırmak.
- Diyabet Yönetimi: Glikoz seviyesindeki artışı algılayıp buna yanıt olarak otomatik olarak doğru miktarda insülin salan “akıllı insülin” sistemleri. Bu, sürekli iğne yapma zorunluluğunu ortadan kaldırabilir.
- Kronik Enflamatuar Hastalıklar: Romatoid artrit gibi hastalıklarda, sadece iltihaplı eklemlere gidip orada anti-enflamatuar ilaçları salan sistemler.
Gelecek Vizyonu: Kapalı Döngü ‘Doktor Çip’ Sistemleri
Akıllı ilaç taşıma teknolojisinin nihai hedefi, kapalı döngü (closed-loop) sistemler yaratmaktır. Bu sistemler, birbiriyle entegre çalışan üç temel bileşenden oluşur:
- Biyosensör: Vücuttaki belirli bir biyobelirteci (örneğin kan şekeri, kanser belirteci) sürekli olarak ölçer.
- İşlemci: Sensörden gelen veriyi analiz eder ve ne kadar ilaca ihtiyaç duyulduğuna karar verir.
- İlaç Taşıyıcı: İşlemciden gelen komutla, tam olarak gereken miktarda ilacı serbest bırakır.
Vücuda yerleştirilebilen tek bir “doktor-çip”, hastalıkları anlık olarak takip edip tedaviye otomatik olarak yanıt verebilir. Bu, gerçek anlamda kişiselleştirilmiş ve otonom tıbbın başlangıcı olacaktır.
Sonuç olarak, nanoteknoloji destekli akıllı ilaç taşıyıcı sistemler, tedavideki kontrol seviyemizi hayal gücümüzün ötesine taşıyor. Pasif bir şekilde hedefe gitmekten, vücudun sinyallerine veya doktorun komutlarına akıllıca yanıt veren sistemlere geçiş yapıyoruz. Bu, yan etkilerin azaldığı, etkinliğin arttığı ve tedavilerin her bireyin kendi biyolojisiyle mükemmel bir uyum içinde çalıştığı bir geleceğin habercisidir.
Yorum yapabilmek için giriş yapmalısınız.


Yazar hakkında